Vivemos em um Universo constituído de matéria e, devido às leis da física, ela se organiza formando padrões e configurações moleculares específicas que são chamadas de estados da matéria. De modo geral, o que determina o padrão - ou estado da matéria - de uma substância são três fatores: a velocidade com que as moléculas se movem, a pressão e a temperatura da substância. Veja que existe uma relação entre os três itens citados, uma vez que a velocidade das moléculas tem relação direta com a temperatura, que por sua vez é relacionada à pressão.
Na escola somos apresentados a apenas três tipos de estados da matéria que são: sólido, líquido e gasoso. Dizem-nos que são esses os estados da matéria. Mas a realidade não é bem assim. Alguns livros escolares, mais atualizados, nos apresentam seis estados da matéria, os citados anteriormente e o plasma, o condensado de Bose-Einstein e o condensado fermiônico. Mesmo com essa modernização por parte dos materiais escolares os livros apenas mostram uma parte da realidade. E esse é o objetivo deste artigo, apresentar ao leitor uma lista menos carente de atualizações e cultivar o interesse particular de cada um pelos fenômenos íntimos da matéria.
A trindade da matéria: sólido, líquido e gasoso
Esses são sem dúvidas os mais conhecidos de todos os estados da matéria. São também os únicos estados possíveis no planeta Terra sem que haja interferência humana. Estes estados da matéria são responsáveis pela formação de vida na Terra e de todas as outras coisas que nela existem.
Começaremos explicando o estado sólido. Este estado, assim como os outros, possui propriedades especiais que o classificam como um estado da matéria. Uma de suas principais características é ter uma forma e volume bem definidos. Isso ocorre devido às condições de pressão e temperatura que fazem com que as moléculas permaneçam unidas. As moléculas então, próximas umas das outras são o que criam a matéria em estado sólido.
O estado líquido da matéria é, assim como o gasoso, parecido com o sólido, exceto por uma coisa: a distância entre as moléculas. No estado líquido as moléculas ainda se encontram próximas umas das outras, mas existe agora certa independência entre elas. Não há mais conjuntos ordenados de moléculas e sim desorganização. É graças a essas propriedades que a água, por exemplo, escapa por nossas mãos ao tentarmos pegá-la, pois as moléculas são independentes umas das outras, o que lhes possibilita escapar por entre nossos dedos.
Os gases são os estados que menos possuem moléculas por unidade de espaço. Por isso não podemos pegar um punhado de ar ou qualquer outro gás. Como as moléculas dos gases estão extremamente afastadas umas das outras, isso confere ao gás a propriedade da compressibilidade. Tal propriedade permite que o gás seja comprimido, ao contrário do que ocorre com líquidos e sólidos, que possuem baixa compressibilidade. Situações extremas com gases fazem com que estes se tornem um outro estado da matéria, que veremos a seguir.
Plasma
O plasma é tido como o quarto estado da matéria. Começou a ser estudado por Michael Faraday em 1830, mas estudos experimentais e teóricos avançados só foram feitos de forma concreta no século seguinte.
Conhecido também como o principal componente das estrelas e dos raios, o plasma é obtido através do superaquecimento de gases. Antes da explicação do que ocorre com o gás para que este se torne plasma, devemos frisar uma propriedade importante da energia térmica. A temperatura de um objeto está relacionada com sua energia térmica que, por sua vez, está relacionada com a quantidade de energia em cada átomo e consequentemente em cada molécula. Devido à ação da temperatura, as moléculas das substâncias ganham uma quantidade de energia proporcional ao valor da temperatura e assim vibram e se agitam de forma intensa.
Imaginemos agora um grande recipiente com o gás hidrogênio e vamos aquecê-lo a milhares de graus célsius. Como vimos anteriormente, essa temperatura dará uma grande quantidade de energia aos átomos do gás. Essa energia irá se acumular no gás, agitando de forma frenética os átomos, fazendo com que estes se movam rapidamente pelo espaço. A colisão destes átomos cria o tipo de ionização mais comum nos plasmas, a ionização colisional. Essas constantes “batidas” que os átomos dão fazem com que estes se ionizem, um deles ganha um elétron e o outro perde, criando uma diferença de cargas no gás, fato que o torna eletricamente condutível.
O plasma das estrelas é formado de uma forma diferente da que os cientistas utilizam para criar plasma aqui na Terra. Nas estrelas, o calor e as colisões das partículas ocorrem devido à enorme pressão da estrela, criada pela sua imensa força gravitacional. A pressão força o gás a se comprimir e obriga os átomos a colidirem. Como os plasmas da Terra, o plasma das estrelas possui enormes propriedades eletromagnéticas. A protuberância vista na direita da foto a seguir é resultado do rompimento de uma linha de campo eletromagnética.
Sem a capacidade de criarmos colossais estrelas para estudar o plasma, somos obrigados a recorrer a outros meios. Nos laboratórios de física experimental, os físicos desenvolveram os chamados Tokamaks, que são enormes reatores de fusão nuclear em forma de rosquinha. Nesses reatores, o plasma é suspenso em uma câmara de vácuo e aquecido a milhões de graus célsius, muitas vezes mais quente que o núcleo do Sol. Este é o gás mais quente que se pode encontrar em nosso sistema solar e em muitos outros. Nessas temperaturas, dentro do plasma, começa o processo conhecido como fusão nuclear, em que os núcleos dos átomos de gás se juntam, formando elementos químicos mais pesados.
Condensado de Bose-Einstein
O estado chamado Condensado de Bose-Einstein é sem dúvida um estado da matéria extremamente exótico, com propriedades que desafiam o senso comum. Seu nome foi dado em homenagem a Albert Einstein que, em 1925, realizou estudos sobre o estado de sistemas quânticos submetidos a temperaturas próximas ao zero absoluto (-273.15 °C), e Satyendra Nath Bose, cujo trabalho na área foi incorporado ao de Einstein, possibilitando assim a criação desse estado da matéria.
Suponhamos, por exemplo, um recipiente com gás. Os átomos e consequentemente as moléculas irão se mover no espaço do recipiente com certa velocidade, determinada principalmente pela temperatura do gás. Com os conhecimentos já adquiridos sobre os demais estados da matéria, sabemos que se resfriarmos o gás primeiramente ele se tornará líquido e logo em seguida sólido. Mas, imagine agora um resfriamento que não seja interrompido até que não haja mais como diminuir a temperatura, ou seja, chegar ao zero absoluto nas escalas de temperatura. Nesse ponto, a matéria age de forma estranha. Os átomos alcançam o menor estado possível de energia na natureza e não possuem mais velocidade. O resultado é que os átomos se empilham e ficam em repouso, sem fazer nada.
Devido a uma das principais regras que rege o mundo quântico, o chamado princípio da incerteza, os átomos (assim como outros elementos quânticos) podem ser descritos com uma função de onda. Tal função não possui nenhum valor físico, porém determina a possibilidade (sim, a possibilidade, pois é impossível saber com precisão absoluta da posição e da velocidade de um elemento quântico no espaço) de encontrar o átomo em certa área. Para uma melhor visualização, vamos imaginar os átomos como pequenas ondas. Enquanto estão no estado sólido, por exemplo, essas ondas não se encostam, o que faz com que cada átomo tenha uma independência, seja uma entidade diferente dos outros. Conforme a temperatura vai diminuindo, as “ondinhas” que imaginamos para representar os átomos vão aumentando de tamanho e ficam mais próximas umas das outras. Eis que finalmente elas se sobrepõem umas às outras. O resultado disso é que os átomos agora podem ser descritos como apenas um grande átomo. Todos os átomos do sistema resfriado compartilham agora das mesmas propriedades quânticas, já não possuem mais identidades diferentes, são apenas um. Como resultado disso, os efeitos quânticos podem ser vistos em escala macroscópica. As antes funções de ondas das quais só podíamos retirar possibilidades inconclusivas, agora são uma única onda com propriedades bem definidas, exatamente como uma onda clássica (por exemplo: onda eletromagnética e sonora).
Superfluido
O estado superfluido era desconhecido na física até 1937, quando Pyotr Leonidovich Kapitsa, um físico russo, descobriu a superfluidez ao congelar o gás hélio a 2,7K (Kelvin, escala de temperatura). O nome que este estado recebeu é um tanto quanto estranho, mas não está exagerado ou equivocado de forma alguma. Na realidade, representa com fidelidade as incríveis propriedades desse estado da matéria. O estado está intimamente ligado ao condensado de Bose-Einstein, pois os superfluidos obedecem à chamada estatística de Bose-Einstein, o que faz com que as partículas obtenham manifestações macroscópicas devido a sua condensação quântica. Isso significa que as propriedades quânticas do material podem ser observadas na escala macroscópica.
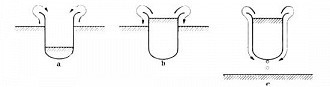
No estado superfluido os átomos estão no mesmo estado quântico, o que possibilita fenômenos interessantes. Uma das coisas notadas nos superfluidos é que sua viscosidade é zero ou muito próxima a zero. Mas por que isso torna o superfluido algo especial? Essa propriedade faz com que, quando derramado em um copo, o superfluido suba pelo copo e caia na mesa na qual este está apoiado. Sim, isso mesmo: o superfluido “escala” as bordas do copo.
Outro fenômeno interessante é a capacidade deste estado da matéria em transportar calor de forma rápida. Nos estados da matéria que estamos habituados (sólido, líquido e gasoso) o calor é normalmente transportado de forma lenta. Percebemos isso quando, por exemplo, vamos nos deitar em um dia frio e demoramos para nos esquentar debaixo da coberta. Se fossemos feitos de superfluidos, iriamos esquentar em segundos. Isso ocorreria porque os líquidos que possuem a chamada superfluidez têm a propriedade de disseminar calor de forma extremamente rápida. Essa propriedade, se utilizada de forma correta, pode possibilitar enormes avanços tecnológicos, em especial em áreas como indústria.
Assim como a transmissão de calor, os superfluidos podem permitir outros fenômenos curiosos. Um desses fenômenos é a disseminação de ondas sonoras de forma extremamente eficiente. As ondas sonoras são ondas mecânicas e por isso podemos ouvir uma perturbação que se propaga em meio material (ar, por exemplo), que será captada pelos ouvidos. Ao que os estudos demonstram, os superfluidos agem de forma magnífica como meios materiais para a propagação de ondas mecânicas.
Fluidos supercríticos
Todo fluido (seja gás ou líquido) quando atinge um ponto específico no diagrama de fases (gráfico que relaciona pressão e temperatura com os estados da matéria) chamado de ponto crítico passa a ser chamado de fluido supercrítico. Esse tipo de estado é muito exótico, sendo normalmente encontrado em indústrias, mas também pode ser encontrado, por exemplo, em vulcões submarinos, onde a temperatura e a pressão são ideias para a formação deste estado da matéria.
Para transformar qualquer fluido em um fluido supercrítico precisamos garantir que ele tenha a temperatura e a pressão certas, ambas acima do ponto crítico do fluido. Quando pressões extremamente altas com temperaturas igualmente altas se combinam, o fluido passa a experimentar características incomuns. Nessas condições o fluido é capaz de se espalhar como um gás e dissolver materiais como um líquido. O material nessas condições já não tem mais as propriedades de gás ou liquido bem definidas, isso vai depender da pressão e da temperatura. Alterando-se a pressão e a temperatura de certa forma podem-se alterar as propriedades do fluido supercrítico, visando que este tenha mais semelhança com um líquido, mas que ainda possa preencher uma caixa, por exemplo, como um gás.
Analisando o diagrama de fases podemos perceber também que não existe mudança de fase entre um gás (ou um líquido) e o fluido supercrítico. Isso significa que a alteração dos estados gasosos e líquidos para o fluido supercrítico ocorre em um processo contínuo. Mas o mesmo não é verdade quando o relacionamos com os materiais sólidos. Com a pressão correta, o fluido supercrítico pode tornar-se um sólido.
Matéria de quarks
É um dos mais complexos estados da matéria de que se tem notícia até hoje. Suas características incomuns, até quando comparadas aos outros estados da matéria, se devem ao fato de ser um estado em que os núcleos atômicos não estão mais coesos.
Sendo de fundamental importância para a física de partículas, a matéria de quarks ou matéria QCD (quantum chromodynamics ou, em português, cromodinâmica quântica) possui exigências tão grandes para existir que, de forma natural, só pôde ser criada no momento da criação do Universo, o big-bang. Hoje em dia somos capazes de produzir o chamado plasma de quarks-glúons em aceleradores de partículas como o RHIC (Relativistic Heavy Ion Collider, em português, colisor de íons pesados relativísticos), que colidem íons de ouro no centro de um detector chamado STAR. Essas colisões geram temperatura e pressão muito elevadas, o que propicia as condições ideais para o plasma de quarks-glúons.
O segredo para o entendimento desse estado da matéria é o conhecimento da cromodinâmica quântica, ou seja, o conhecimento das interações sofridas por partículas que possuem carga de cor (quarks). A força nuclear forte, responsável pela coesão nuclear, é a personagem principal no plasma de quarks-glúons. Essa força aprisiona os quarks, juntando-os em conjuntos estáveis como hádrons (prótons e nêutrons) e mésons (par de quark e antiquark). Esse aprisionamento, tecnicamente chamado de emparelhamento, é o que mantem a matéria unida e garante estrutura para todas as coisas, pois quarks unidos formam prótons e nêutrons que, por sua vez, formam núcleos átômicos, que por sua vez, formam moléculas que, finalmente, quando combinadas em grandes quantidades, formam as estruturas macroscópicas as quais estamos acostumados.
O emparelhamento que ocorre naturalmente na matéria normal é desfeito no plasma de guarks-glúons. Isso significa que, de forma simplória, os quarks e glúons (partículas que mediam a força forte, ou seja, “colam” os quarks) ficam quase todos livres, sem estarem emparelhados, formando estruturas hadrônicas. Podemos dizer, então, que esse plasma é um estado da matéria onde a maior parte de seu material não apresenta estruturas atômicas normais, pois elas teriam sido “destruídas” quando houve o desemparelhamento de seus quarks. Teoriza-se que esse estado da matéria se fez presente durante o big-bang (momento de criação do universo) devido à enorme temperatura e densidade em que este se encontrava (bilhões e bilhões de graus Célsius). Quarks isolados nunca foram observados por dois motivos: o primeiro é que seu emparelhamento, efeito criado pela força nuclear forte, é extremamente difícil de romper e, mesmo que isso seja feito, os quarks iriam decair, criando outras partículas, pois são extremamente instáveis sozinhos. Sua existência desemparelhada no plasma de guarks-glúons existe devido a uma série de complexos fenômenos descritos pela cromodinâmica quântica.